马明团队利用生物合成和化学修饰制备新颖套索肽类天然产物

2021年8月10日,我室马明研究团队在英国皇家化学会旗舰刊《Chemical Science》在线发表了题为“Rational Generation of Lasso Peptides Based on Biosynthetic Gene Mutations and Site-Selective Chemical Modifications”的研究论文,报道了一类独特的套索肽天然产物的发现,以及利用生物合成基因突变和位点选择性化学修饰制备套索肽衍生物的研究成果。
套索肽(lasso peptides)是一类结构独特的天然产物,结构中常含有14-33个氨基酸残基,其N端第1个氨基酸与第7,8或者第9个氨基酸侧链形成大酰胺环,而C端的氨基酸穿过此大酰胺环,形成标志性的“套索”结构。此“套索”结构具有极强的热稳定性和蛋白酶解稳定性,因此套索肽被认为是具有理想药代动力学性质的潜在药用分子。根据是否含有二硫键以及二硫键的连接位置,目前已经发现四类套索肽。目前发现的天然套索肽具有抗菌、抗肿瘤、抗HIV等作用;更有意思的是通过生物合成基因突变方式将整合素(integrins)的三肽识别序列Arg-Gly-Asp引入到套索肽MccJ25中后,发现此MccJ25衍生物具有抑制人脐静脉内皮细胞血管形成作用。因此,套索肽本身、或者依托套索肽高稳定性的骨架缀合药用功能分子,在先导药物开发方面具有广阔的空间。
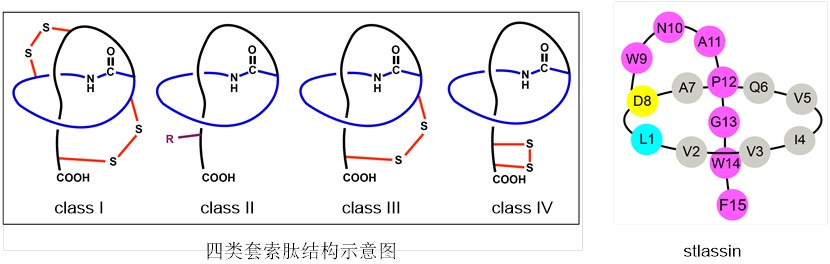
图1. 套索肽的四类结构示意图和本研究发现的新颖套索肽stlassin结构
然而,目前套索肽相关研究受到了几个方面的限制:由于独特的三维“套索”结构难以化学合成,导致无法像其它肽类化合物那样用固相多肽合成方法制备化合物库;套索肽生物合成基因簇常处于沉默状态,限制了天然套索肽分子的大量发现;另外,虽然有针对套索肽生物合成基因簇异源表达(主要在E. coli中)的研究报道,但此类研究大多数产生的套索肽产量低,无法满足结构修饰和生物活性测试的要求。
针对上述问题,马明研究团队首先从一株海洋链霉菌(来自于团队所构建的海洋细菌菌种库)中发现了一个套索肽生物合成基因簇stla,通过将stla克隆至链霉菌Streptomyces coelicolor A3(2)中进行异源表达,并引入KasOp*启动子激活该基因簇,成功发现一个新颖的II型套索肽stlassin,计算产量可达20 mg/L。基于该异源制备平台,研究团队对stlassin生物合成中前体肽中的核心肽(15个氨基酸残基)开展了点突变,发现核心肽中15个氨基酸位置的突变对生物合成具有不同的影响;同时得益于异源制备平台的高产量以及生物合成中翻译后修饰酶对前体肽突变的容忍性,制备了17个相应的stlassin突变体分子。对stlassin及其变体分子进行了溶液核磁共振结构测定,确证了它们独特的右手螺旋“套索”结构。同时stlassin及其变体分子显示了极高的稳定性,实验证实它们可以对抗95 °C加热以及carboxypeptidase Y的酶解。
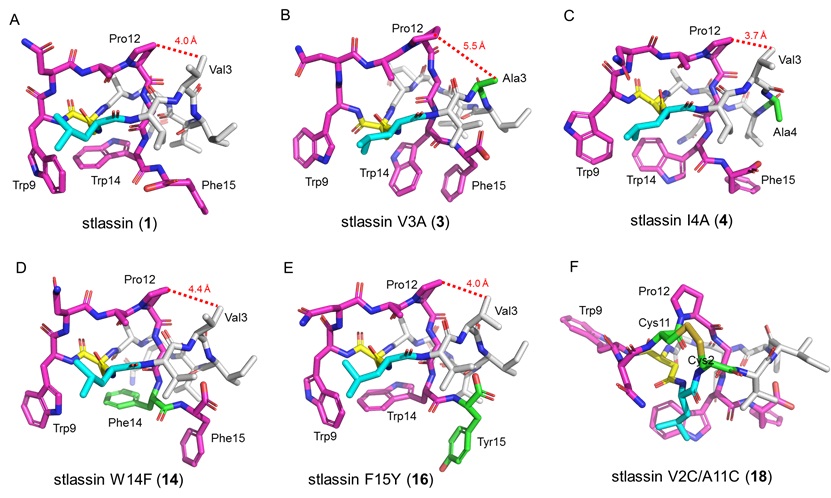
图2. Stlassin及其变体分子的溶液核磁共振三维结构
除了利用生物合成前体肽基因突变获得stlassin变体分子外,研究团队还结合近年报道的蛋白/多肽位点选择性修饰反应,进一步扩展stlassin类分子结构多样性。通过生物合成前体肽基因突变和高产量异源制备平台,成功得到了引入酪氨酸或者半胱氨酸残基的stlassin变体分子。针对引入的酪氨酸或者半胱氨酸侧链活性基团进行多种温和条件下的高效修饰反应,制备了10个包含O-糖基化、S-糖基化、S-芳香化、分子内二硫键、分子间二硫键、硫消除及巯基分子加成等修饰的stlassin变体分子。部分变体分子结构已经超越了目前对套索肽的四种分类范围。值得注意的是这些修饰反应弥补了生物合成中相应修饰基因缺失的不足,将生物合成制备“套索”骨架与骨架的化学修饰相结合,体现了“源于自然,优于自然”的天然产物变体分子制备理念。研究团队最后对所得stlassin及其变体分子开展了生物活性测试,发现它们不同程度的抑制脂多糖(LPS)与Toll-like receptor 4 (TLR4)受体的结合,表现出抗炎活性的潜力。
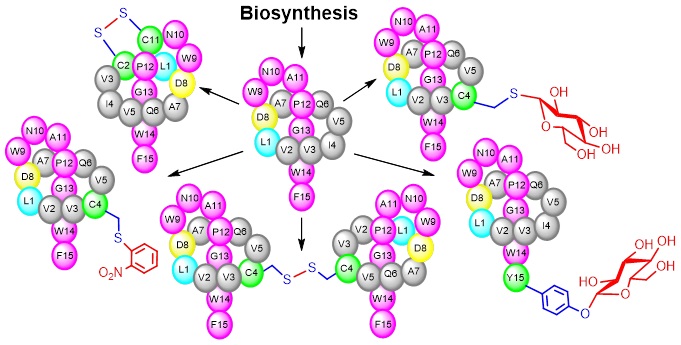
图3. 生物合成和化学修饰相结合扩展套索肽结构多样性
该项工作得到科技部重点研发计划“深海关键技术与装备”项目“重要深海药源天然产物合成生物学产生体系构建”、国家自然科学基金委等资助。北京大学药学院博士研究生刘谈、马晓杰为本论文共同第一作者,中国科学院生物物理研究所蛋白质核磁研究平台的刘雪辉老师和北京大学药学院马明研究员为共同通讯作者。同济大学韩华老师及杨文盛同学在生物活性测试方面提供了支持。


刘谈 博士 马晓杰 博士
原文链接:https://doi.org/10.1039/D1SC02695J
【通讯作者简介】

马明,北京大学药学院、天然药物及仿生药物国家重点实验室研究员,博士生导师,Tenure-Track助理教授。研究领域为天然药用功能分子的生物合成,酶的三维结构及其催化机制,以及天然产物合成生物学。近5年以通讯作者在JACS、Chem. Sci.、Org. Lett.、J. Biol. Chem.、J. Org. Chem.、J. Nat. Prod.、Chin. J. Chem.、 Appl. Microbiol. Biotechnol.、ACS Omega、Mar. Drug等国际学术期刊发表论文十余篇。任中国药学会海洋药物专业委员会委员、中华中医药学会青年委员会委员、北京药学会天然药物专业委员会委员。

