张宏权教授研究团队发现肺腺癌转移和耐药的新机制
2019年4月6日,我室张宏权教授研究团队在国际知名转化医学期刊Theranostics发表论文,报道了肺腺癌侵袭转移与化疗耐药的新分子机制。这项历时近6年的研究发现同源异形盒转录因子HOXB13促进肺腺癌侵袭、转移与对化疗耐药的新机制。论文题目为“HOXB13 networking with ABCG1/EZH2/Slug mediates metastasis and confers resistance to cisplatin in lung adenocarcinoma patients”。研究团队的战军副教授为论文第一作者,张宏权教授为责任作者。该研究得到国家癌症中心暨协和肿瘤医院内科主任医师王洁教授研究团队的协助。
转移、耐药和复发是恶性肿瘤在临床治疗上的三大难题。张宏权教授目前担任中国解剖学会副理事长、中国抗癌协会肿瘤转移专业委员会的侯任主任委员、中国抗癌协会血液转化医学专业委员会常委及中国抗癌协会肺癌专业委员会委员,他领导的研究组长期从事肿瘤侵袭、转移及耐药的分子机制研究。
上述长达16页的研究论文揭示出在发育上起重要作用的同源异形盒转录因子HOXB13,通过靶向促癌基因EZH2/ABCG1/Slug信号轴并上调其表达,促进肺腺癌的侵袭、转移及对顺铂耐药;该研究同时揭示出肺腺癌原发性耐药与化疗后继发耐药的分子机制,为患者化疗前耐药预测、生存期判断提供了科学而灵敏的检测方法,也为研发抵抗化疗耐药的新药创制提供了新的潜在靶点。
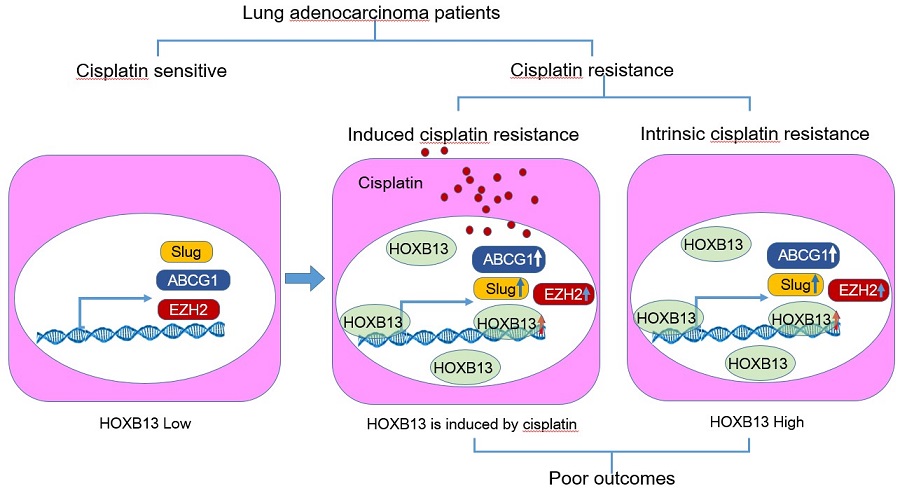
HOXB13与ABCG1、EZH2及Slug形成网络调节肺腺癌的转移并导致肺腺癌病人对顺铂治疗的耐药
肺癌的转移和耐药是其治疗失败、生存期短的主要原因,尤其是继发耐药使本来有效的治疗变得失败。张宏权教授研究团队首先在肺腺癌耐药患者组织中发现同源异形盒转录因子HOXB13表达异常上调,并且HOXB13表达的增高对应着患者癌组织更差的临床分期和更不良的预后。继而研究团队对于HOXB13的生物学功能进行了详细解析,发现高表达HOXB13的细胞具有更强大的增殖能力和运动侵袭能力,并具有更强的耐药性。这些细胞到了动物体内表现出更早的成瘤能力及强大的局部侵袭和远隔器官转移能力。研究团队在全基因组范围内检测了HOXB13可能的下游靶基因,并对每个靶基因进行了逐一验证,确定了其中ABCG1、EZH2、Slug及HOXB13自身是受HOXB13 直接靶向并上调的下游分子。ABC转运体ABCG1和重要表观遗传调控因子EZH2与启动子结合而产生耐药性;而EZH2和Slug是HOXB13促迁移侵袭的调控分子;同时HOXB13通过自身正反馈调节形成更强大的调节环路使其生物学功能再度被放大。更为重要的是研究团队发现顺铂在癌细胞和患者来源的移植物(PDX)中能够显著诱导HOXB13的表达上调。因此,该发现是化疗继发耐药的关键机制,也是控制肺腺癌继发耐药的有效靶点。联合应用HOXB13及其靶向基因ABCG1和EZH2比单分子应用获得更有效的预测患者对基于铂类药物治疗的敏感性、治疗效果和患者预后,从而可作为临床监测肺腺癌患者耐药性和预测预后的备选指标。该研究已经申请国家专利局专利。上述发现得到Theranostics资深编辑和论文审稿人的认同,论文同时获得高度评价。
该工作得到了国家自然科学基金重点项目、国家科技部重大基础研究专项、北京市自然科学基金重点项目及北京大学重点基础研究专项的资助。
论文链接:http://www.thno.org/v09p2084.htm
【张宏权教授简介】

张宏权教授长期从事跨膜受体整合素胞内结构域相互作用蛋白所介导的肿瘤增殖、侵袭、转移和网络调控的分子细胞生物学机制,肿瘤细胞重编程产生肿瘤干细胞及其在肿瘤复发和转移中的作用机制研究。近年来,发现整合素相关蛋白Kindlin-2 对调控抗癌药物顺铂敏感性、激活Wnt 信号通路、调控EMT 及肾脏纤维化等方面起重要作用。还发现乙酰化的组蛋白甲基转移酶EZH2 可增加自身稳定性,在肺腺癌预后中起作用。在Cell, Cell Stem Cell, Cell Res., Nat. Cell Biol., Mol. Cell, J. Cell Biol., EMBO Reports, PNAS, Nucleic Acids Res., Mol. Cell Biol. 等杂志发表论文60 余篇。
(编辑:宋书香 供稿:基础医学院)

